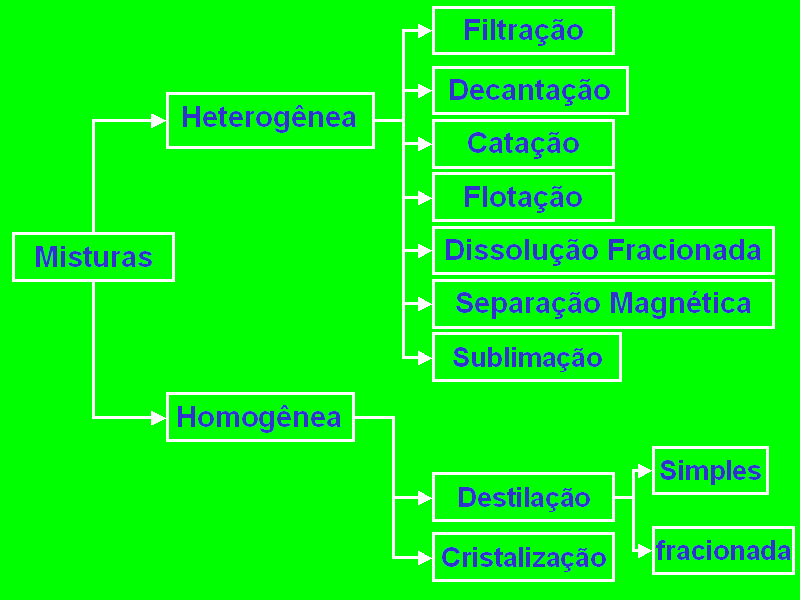
Misturas homogêneas e heterogêneas
Material homogêneo
Um único aspecto no ultramicroscópio;
Todas as suas porções apresentam as mesmas propriedades
Fase: cada porção homogênea (contínua ou não) de um material.
Homogêneo apresenta somente uma fase.
Ex: álcool, ouro 18K (75% de Au e 25% de Cu e/ou Ag), solução de água e açúcar.
Heterogêneo apresenta mais de uma fase.
Ex: água e óleo, leite, sangue.
Separação de misturas
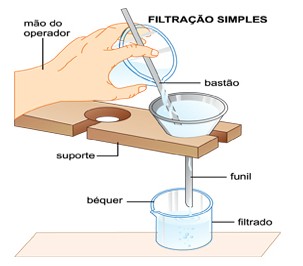
Filtração: A separação se faz através de uma superfície porosa chamada filtro; o componente sólido ficará retido sobre a sua superfície, separando-se assim do líquido que atravessa.
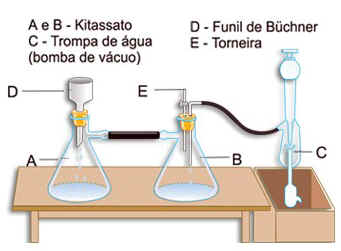
Filtração à vácuo: A filtração pode ser acelerada pela rarefação do ar, abaixo do filtro. Nas filtrações sob pressão reduzida, usa-se funil com fundo de porcelada porosa (funil de Büchner)
Decantação: Deixa-se a mistura em repouso até que o componente sólido tenha-se depositado completamente. Remove-se em seguida, o líquido, entornando-se cuidadosamente o frasco, ou com auxílio de um sifão (sifonação).
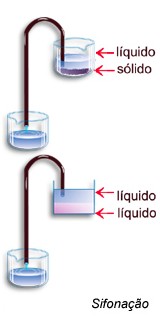
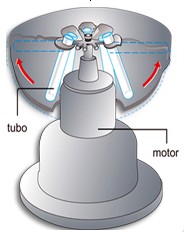
Para acelerar a sedimentação do sólido, pode-se recorrer à centrifugação, conforme o desenho:
.
A decantação é muito utilizada para separar líquidos imiscíveis, ou seja, líquidos que não se misturam. Para isso, coloca-se a mistura a ser separada em um funil de separação (ou funil de decantação ou funil ed bromo). Quando a superfície de separação das camadas líquidas estiver bem nítida, abre-se a torneira e deixa-se escoar o líquido da camada inferior, conforme o desenho:
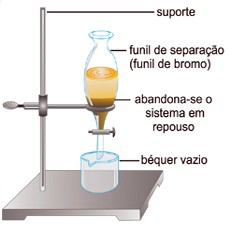
Quando os líquidos não se separam pelo simples repouso, ou o fazem muito lentamente, submete-se inicialmente a mistura à centrifugação.

Dissolução Fracionada: Trata-se a mistura com um líquido que dissolva apenas um dos componentes. Por filtração, separa-se o componente não-dissolvido; por evaporação (ou destilação) da solução, separa-se o componente dissolvido no líquido. Veja o exemplo a seguir:
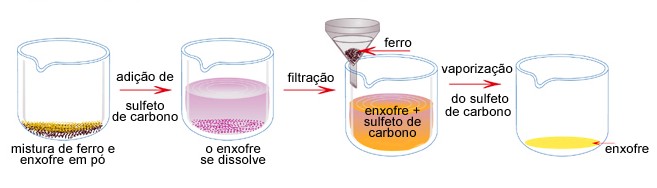
Sublimação: Só pode ser aplicada quando uma das fases sublima com facilidade. É empregada na purificação do iodo e do naftaleno.

Flotação: Trata-se a mistura com um líquido de densidade intermediária em relação às dos componentes. O componente menos denso que o líquido flutuará, separando-se assim do componente mais denso, que se depositará. O líquido empregado não deve, contudo, dissolver os componentes. Também é denominado de sedimentação fracionada. Veja o exemplo:

Cristalização fracionada: A mistura de sólidos é dissolvida em água e a solução é submetida à evaporação. Quando a solução ficar saturada em relação à um componente, o prosseguimento da evaporação do solvente acarretará a cristalização gradativa do referido componente, que se separará da solução. A solução, contendo o componente cuja saturação ainda não foi atingida, fica sobre os cristais do outro e é chamada água-mãe de cristalização.
Separação magnética: Só pode ser usada quando um dos componentes é atraído por um imã. Veja:

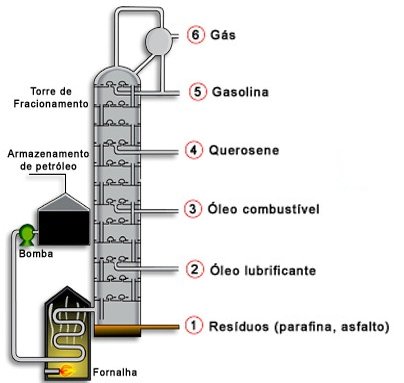
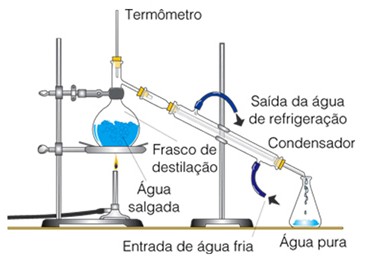
Destilação simples: para a separação dos componentes das misturas homogêneas sólido-líquido, recorre-se comumente a destilação simples. O princípio do processo consiste em aquecer a mistura até a ebulição; com isso o componente líquido separa-se do sistema sob a forma de vapor, que a seguir é resfriado, condensando-se, e o líquido é recolhido em outro recipiente. Veja:
Destilação fracionada: para a separação dos componentes das misturas homogêneas líquido-líquido, recorre-se comumente à destilação fracionada. Aquecendo-se a mistura em um balão de destilação, os líquidos destilam-se na ordem crescente de seus pontos de ebulição e podem ser separados. O petróleo é separado em suas frações por destilação fracionada. Veja: